细胞平台
多篇文章共同解读癌细胞的“狡诈”特性!

(PDL-1外泌体)
【1】Science子刊:重磅!在人类癌症患者中,癌细胞与免疫细胞融合在一起
doi:10.1126/sciadv.aat7828
一个多世纪以前,德国病理学家Otto Aichel吃惊地观察到癌细胞具有不同细胞类型(包括白细胞)的特征。这些数据让他提出癌细胞和白细胞之间的融合能够给肿瘤带来优势,使得它更容易在体内扩散。但是从那以后,人们很难找到癌细胞和免疫细胞融合在一起形成杂合体(hybrid,即下文中的hybrid cancer cell,也可译为杂合癌细胞)的证据。
如今,Aichel的这一理论得到了更多的支持。在一项新的研究中,来自美国俄勒冈健康与科学大学的研究人员在癌症小鼠模型中和在实体瘤患者的外周血中发现了这种杂合体的存在。相关研究结果发表在2018年9月12日的Science Advances期刊上。
【2】EMBO J:揭开困扰科学家的百年难题!为何癌细胞会选择无效的方式生长繁殖?
doi:10.15252/embj.201899735
近一个世纪以来,科学家们在癌细胞中观察到了一种奇怪的行为,即癌细胞更喜欢利用低效率的通路来产生能量,正常细胞能够利用有氧糖酵解的方式使用普天堂来产生36个储存能量的ATP分子,而大部分癌细胞尽管在氧气存在的情况下,其也会选择开启无氧糖酵解的方式来产生两个ATP分子。
这就是所谓的沃伯格效应,该过程依赖于一类名为乳酸脱氢酶的特殊酶类,而其中的乳酸脱氢酶A(LDHA)是最突出的成员之一,抑制LDHA就能够阻断癌细胞产生其生长和生存所需要的能量,但研究人员并不清楚如何能更加有效地抑制LDHA,很大程度上是因为缺乏能在体内发挥作用的药理学抑制剂。
近日,一项刊登在国际杂志EMBO Journal上的研究报告中,来自Sanford Burnham Prebys医学探索研究院的科学家们利用遗传学和药理学方法进行研究发现,阻断LDHA或许仅会对黑色素瘤细胞产生有限的效应,因为其会被更改能量的产生;文章中,研究人员鉴别出了一种由ATF4分子驱动的替代生长通路,同时也揭示了一种药物开发的潜在新型靶点。
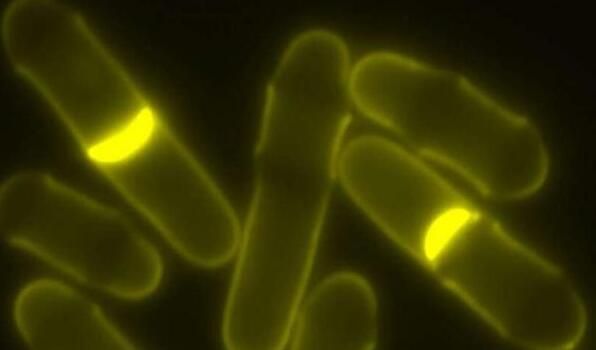
【3】Gene Dev:揭开癌细胞复制的秘密
doi:10.1101/gad.311910.118
南卡罗来纳医科大学霍林斯癌症中心的科学家发现,一些细胞可以在必要因子存在的情况下分裂。他们的结果发表在2018年7月的《Gene & Development》杂志上。这一发现解释了肝细胞在受伤后如何再生,以及可以帮助我们了解癌症是如何产生的,以及癌细胞如何进化以产生额外的突变,从而加速生长和扩散。
该论文的作者包括Hollings癌症中心主任Gustavo Leone博士等人。Leone实验室的重点领域之一是研究正常细胞如何分裂以更好地了解癌细胞中的过程,癌细胞可快速分裂并扩散。
作者解释说,细胞分裂在生长期间(例如胚胎发育以及替换死亡或受损细胞)是必要的。细胞分裂的关键是精确复制每个染色体,为每个产生的细胞提供相同的DNA,称为DNA复制。在此过程中发生的错误可导致细胞具有异常的染色体拷贝或导致癌症发生的有害突变。“我们是多细胞生物,”作者说道, “对于多细胞生物来说,细胞复制很重要,因此DNA复制也同样非常重要。”
【4】Nature:重磅!揭示癌细胞抑制抗肿瘤免疫反应新机制-从远处释放携带PD-L1的外泌体
doi:10.1038/s41586-018-0392-8
癌细胞并不仅仅是一群生长失去控制的细胞;为了自身的生存,它们积极地参与与免疫系统之间的斗争。能够逃避免疫系统检测是癌症的一种特征。在一项新的研究中,来自美国宾夕法尼亚大学的研究人员发现癌细胞释放生物“无人机”---在血液中循环的被称作外泌体(exosome)的小囊泡,这些小囊泡携带着PD-L1蛋白,这种蛋白导致T细胞在到达肿瘤并进行战斗之前精疲力竭---来协助这种斗争。尽管这项研究主要针对转移性黑色素瘤,但是这些研究人员发现乳腺癌和肺癌也会释放携带着PD-L1的外泌体。相关研究结果于2018年8月8日在线发表在Nature期刊上。
这项研究以一种颠覆现有观念的方式展示了癌症如何采取一种系统性方法来抑制免疫系统。此外,它还指出了一种新方法来预测哪些癌症患者会对通过破坏免疫抑制来抵抗肿瘤的抗PD1疗法(anti-PD1 therapy)作出反应,并提供一种追踪这类疗法治疗效果的方法。
Guo说,“对许多转移性黑色素瘤患者来说,免疫疗法可以挽救生命,但是大约70%的这些患者没有作出反应。这类疗法费用昂贵并且具有毒副作用,因此了解哪些患者会作出反应将是有帮助的。鉴定血液中的生物标志物可能有助于及早预测哪些患者会作出反应,以及随后可能为患者及其医生提供一种监测治疗效果的方法。”
【5】Cancer Cell:死了都要癌!死亡的癌细胞竟会使活着的胶质瘤细胞更耐药
doi:10.1016/j.ccell.2018.05.012
像GBM这样的恶性肿瘤中持续增殖的肿瘤细胞周围掺杂着许多凋亡的细胞,但是研究人员此前并没有注意过这些凋亡细胞和活细胞之间的细胞间信号交流。在近日一项发表在《Cancer Cell》上的研究中,来自阿拉巴马大学伯明翰分校的研究人员发现凋亡的GBM细胞竟然可以通过分泌富含不同剪接体组分的apoEVs来促进存活的GBM细胞持续增殖,并提高它们耐受治疗的能力。
apoEVs会改变受体GBM细胞的RNA剪接,因此促进这些细胞向着更耐药、更恶性、更容易迁移的表型转变。
通过机理研究,研究人员发现RBM11是肿瘤治疗后显著上调的代表性剪接体因子,一旦肿瘤细胞发生凋亡它就会富集在apoEVs中。一旦这些apoEVs被受体GBM细胞吞噬,这些外源性RBM11就会改变MDM4和细胞周期蛋白D1的剪接状态,使它们表达出更致癌形式的蛋白质,从而使得这些GBM细胞更耐受治疗,恶性程度更高。
【6】Cell Metabol:不光依赖于血管发生 癌细胞还能利用脂质分子进行生长扩散
doi:10.1016/j.cmet.2018.05.005
近日,一项刊登在国际杂志Cell Metabolism上的研究报告中,来自瑞典卡罗琳学院等机构的研究人员通过研究发现,当血液供应不足时,癌细胞就能使用脂质分子作为燃料而并非血糖,这一机制或能帮助解释为何肿瘤通常会对抑制血管生成的癌症药物产生耐药性。
肿瘤的生长和扩散依赖于血管发生,而血管发生即新血管生成的一种过程,其能够为癌细胞供给营养物质和激素,包括葡萄糖等;利用抗血管生成的药物就能够减少肿瘤中血管的数量以及供给癌细胞的葡萄糖供应水平,如今研究人员开发出了多种类似的药物来治疗多种类型的癌症患者,然而抗血管生成药物在癌症患者中的临床效益普遍较低,而且癌症通常会对疗法产生一定的耐药性,尤其是一些接近脂肪组织生长的癌症类型,比如乳腺癌、胰腺癌、肝癌和前列腺癌等。
【7】Science:重磅!结肠癌细胞携带着细菌一起在体内转移
doi:10.1126/science.aal5240
在一项新的研究中,来自美国哈佛大学等研究机构的研究人员发现证据表明在结肠癌肿瘤中发现的某种类型的细菌与结肠癌细胞一起转移到身体其他部位时会侵入那里的肿瘤中。在他们于2017年11月23日在线发表在Science期刊上的一篇标题为“Analysis of Fusobacterium persistence and antibiotic response in colorectal cancer”的论文中,他们研究了这种细菌及其与结肠癌的病因之间可能存在的关联性。
之前的研究已表明细菌与肿瘤细胞一起存在于多种癌症中,这就导致医学领域的一些人想要知道它们是否实际上是肿瘤形成的原因。已有人发现一种这样的细菌,即具核梭杆菌(Fusobacterium nucleatum),与结肠癌细胞一起存在着。在这项新的研究中,这些研究人员想要知道这种细菌是否可能与已迁移到身体其他部分(特别是肝脏)中的结肠癌细胞一起存在着。
【8】JCS:来自癌细胞内部的信号分子如何促进癌症恶性进展?
doi:10.1242/jcs.208926
癌细胞的外部常常会被信号所“攻击”,这些信号来自免疫系统,其能支持组织和其它结构发挥正常功能,那么这些信号如何影响癌症进展呢?近日,一项刊登在国际杂志Journal of Cell Science上的研究报告中,来自密歇根大学的科学家们通过研究提供了一种特殊的过程模型来阐明这些信号是如何进入并且影响细胞的,相关研究或能帮助研究人员开发抵御癌症的新型疗法。
研究者Sofia Merajver博士说道,这项研究中,我们阐明了这些信号如何进入细胞内部从而影响癌细胞的多个方面,即癌细胞如何通过增殖和移动来产生反应的,研究者发现了癌细胞吞咽特殊分子以及这些分子激活肿瘤抑制基因之间的特殊关联,基于前期研究结果,这项研究中,研究人员重点对一种名为网格蛋白的蛋白质进行研究,网格蛋白能够影响代谢产物、激素和其它蛋白质进入到细胞中,而网格蛋白小窝(clathrin-coated pits)则能在细胞表面形成小凹痕,从而被细胞内化。
【9】Open Biol:癌细胞如何在营养不良的状况下生长繁殖?
doi:10.1098/rsob.180015
癌症研究领域的其中一个秘密就是肿瘤细胞如何在血液和营养状况不良的情况下存活并且生长,近日,来自弗林德斯大学和纽卡斯尔大学的科学家们通过研究系统性地绘制了相关的核心基因图谱和生物学图谱来解释癌细胞如何在营养压力状况下得以生存并繁殖,相关研究刊登于国际杂志Open Biology上。
文章中,研究人员提出了一套针对细胞和生物学过程的新型数据,其或许能够帮助调节癌细胞在不良营养状况下生存的能力特性,研究者利用高通量的筛选技术识别出了能够调节细胞适应性的关键基因,Petersen教授表示,对这些数据进行综合性收集及分析还能帮助其他研究人员寻找肿瘤生长的路径。
【10】Cell Rep:防癌卫士p53也会帮助癌细胞 避免发生铁死亡
doi:10.1016/j.celrep.2017.12.077
癌细胞如何应答营养匮乏目前仍然不是特别清楚。在某些癌细胞内,半胱氨酸的缺乏会诱导铁依赖性细胞死亡,叫做铁死亡(ferroptosis),这种细胞死亡方式不同于细胞凋亡。最近的一些证据表明铁死亡的敏感性可能受到应激应答转录因子和经典肿瘤抑制因子p53的调节。
为了进一步揭示肿瘤抑制因子p53与铁死亡敏感性的关系,来自美国斯坦福大学医学院的研究人员利用CRISPR/Cas9基因组编辑、小分子探针以及高分辨率延时成像等技术进行了相关研究。研究结果发表在国际学术期刊Cell Reports上。
(本文来源生物谷)
想要了解更多请关注“中洪博元医学实验帮 ”
上海展辉生物技术有限公司
地址:上海市浦东新区东方路
联系电话:400-689-6719
联系邮箱:3369352092@qq.com
联系我们:
4006896719

扫一扫
关注东洪博元更多动态