医学行业动态
今日,Genmab宣布了其3期临床试验ALCYONE的顶线数据。该试验是评估daratumumab与bortezomib、melphalan和prednisone(简称VMP)联合用于一线治疗多发性骨髓瘤患者,这些患者不能进行自体干细胞移植(ASCT)。预先计划的中期分析显示,试验到达了主要研究终点。
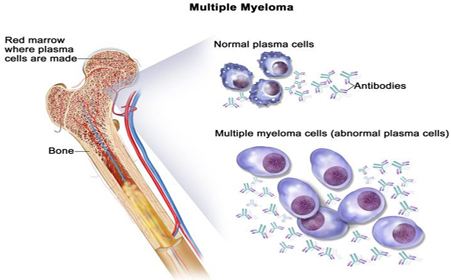
多发性骨髓瘤是一种无法治愈的血液癌症,起始于骨髓,表现为血浆细胞过度增殖。多发性骨髓瘤是美国第三常见的血癌,仅次于白血病和淋巴瘤。近期的数据显示,2016年在美国约有30330个新病例出现,约12650人死于该疾病;在全球范围内,2015年约有124225个新病例出现,87084人死于该疾病。虽然一些多发性骨髓瘤患者没有症状,但大多数患者会由于骨问题、低血象、钙升高、肾脏问题等被诊断出来。经过标准治疗(包括蛋白酶体抑制剂或免疫调节剂)后复发的患者,预后很差,几乎没有可用的治疗方案。这些患者急需新的治疗方案来帮助延长生命。
Daratumumab就是这样一款充满潜力的药物。作为一种人源IgG1k单克隆抗体(mAb),它以高亲和力与CD38分子结合,该分子在多发性骨髓瘤细胞表面高度表达。然后daratumumab触发人体自身的免疫系统来攻击癌细胞,除了直接导致癌细胞凋亡外,还通过多种免疫介导的机制和免疫调节作用快速杀死癌细胞。它已获美国FDA批准,单独使用或与来那度胺(lenalidomide)和地塞米松(dexamethasone)或硼替佐米(bortezomib)和地塞米松(dexamethasone)联合使用,治疗多发性骨髓瘤。它是首个获批的靶向CD38的单抗药物。
Daratumumab的疗效和安全性在临床试验中也得到了验证。在这项随机、开放标签、多中心的3期临床试验中,706名新诊断且无法进行自体干细胞移植的多发性骨髓瘤患者被随机分配,分别接受daratumumab与VMP组合治疗或VMP单独治疗。联合治疗组的患者接受每周一次16 mg/kg的daratumumab治疗,持续6周,作为一个疗程。然后每3周进行一次治疗,共进行9个疗程。完成总共9个疗程后,患者会继续接受16 mg/kg的daratumumab治疗,每4周一次,直到疾病进展。该试验的主要终点是无进展生存期(PFS)。
结果显示,与单独使用VMP治疗的患者相比,加入daratumumab治疗降低了疾病进展风险或死亡约50%(HR=0.50, [95%CI: 0.38-0.65], p<0.0001),到达了主要终点。联合治疗组的中位PFS还未达到,而VMP治疗组的中位PFS约为18.1个月。该联合疗法的安全性与VMP疗法和daratumumab的安全性一致。
基于以上结果,独立数据监测委员会(IDMC)建议数据进行非盲化。所有患者会继续被监测记录安全性和总生存期。具体数据会在即将召开的医学会议及同行评议的期刊上发表。从Genmab获得该药物授权的Janssen Biotech将与监管部门进行沟通,讨论递交该适应症的监管文件。
“ALCYONE研究的中期结果再次证明了daratumumab与已有治疗方案联合治疗多发性骨髓瘤的潜力,这次是与VMP联合作为一线治疗。我们对本研究预先计划的中期分析结果感到非常满意,这进一步增加了我们的希望,daratumumab有可能成为重新定义多发性骨髓瘤联合治疗的关键驱动力,”Genmab首席执行官Jan van de Winkel博士说。
(本文转载生物谷)
上一篇:肠道菌群随季节改变
下一篇:脂肪肝可影响其它组织的正常功能
上海展辉生物技术有限公司
地址:上海市浦东新区东方路
联系电话:400-689-6719
联系邮箱:3369352092@qq.com
联系我们:
4006896719

扫一扫
关注东洪博元更多动态