Carl June团队最新研究:CAR-T细胞离体培养时间缩短至三天,抗肿瘤活性更强大
现如今,嵌合抗原受体(CAR)介导的急性淋巴细胞白血病(ALL)免疫治疗的已经成功突出了靶向特定肿瘤抗原的细胞毒性T细胞疗法的潜力,而CAR-T细胞疗法的有效性取决于过继转移后T细胞的植入和持久性。
(CAR-T细胞离体培养)
CAR-T大牛(从左至右):Bruce Levine, Stephan Grupp, Carl June, Joseph Melenhorst
目前,大多数T细胞工程化方案通常是将T细胞离体扩增9-14天。因为植入和持久的可能性与T细胞分化的状态有关,Carl June等人假设减少离体培养的持续时间能够限制分化并增强CAR-T细胞疗法的抗癌活性。
敲 · 黑 · 板
最终,研究人员证明了相比较于较晚(第9天)的时间点,靶向CD19的CAR-T细胞(CD19-BBζCAR,与宾夕法尼亚大学的CTL019试验中使用的结构相同)在较早(第3天或第5天)的培养时间点,表现出较少的分化以及增强的效应子功能。
然后研究人员比较了早期与晚期收获的CART19在ALL小鼠异种移植模型中的治疗潜力,结果显示抗白血病活性与CAR-T细胞离体培养时间呈负相关:尽管使用的是低6倍剂量的CART19,第3天收获的细胞仍能显示出强大的抗肿瘤活性,而第9天收获的细胞在限制的细胞剂量下并不能控制白血病进展。
此外,该研究团队还证明了在大规模cGMP生产条件下,简化细胞培养的可行性。综上所述,限制T细胞分离提取到实施CAR治疗之间的时间间隔对于疾病进展迅速的患者至关重要。
Yescarta(CAR-T/Kite)的完整制备时间为17天;Kymriah(诺华)的完整制备时间为3到4周
而且在更短的时间内完成CAR-T细胞的制备也可以提高效力,以有助于CAR-T疗法最大限度的发挥其抗肿瘤活性。
研究结果展示
1. 在离体培养期间,T细胞随时间逐渐分化
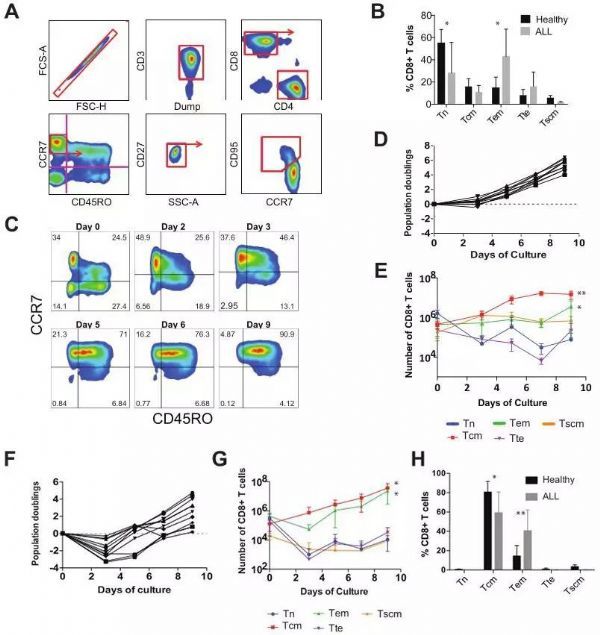 2. 在体外试验中,早期收获的CART19细胞在抗原暴露后显示出增强的效应子功能和增殖能力
2. 在体外试验中,早期收获的CART19细胞在抗原暴露后显示出增强的效应子功能和增殖能力
 3. 早期收获的CART19细胞在体内显示出更有效和持久的抗肿瘤反应
3. 早期收获的CART19细胞在体内显示出更有效和持久的抗肿瘤反应
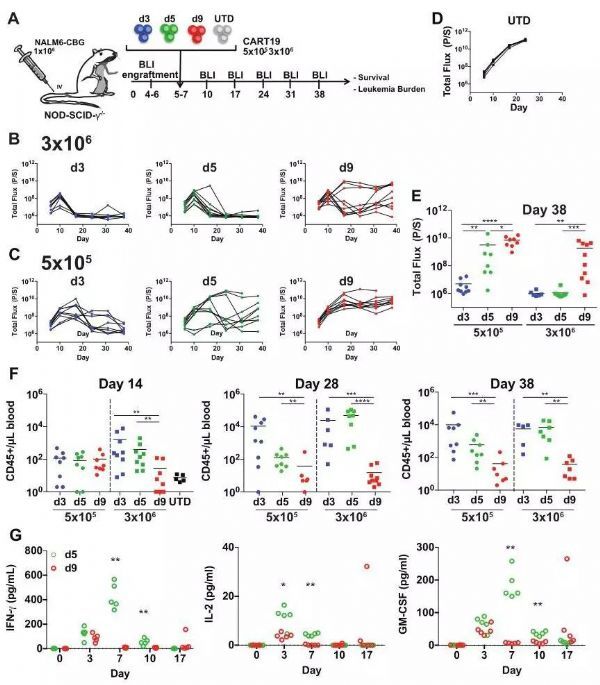 4. 在GMP大规模生产设施中,一种简化的CAR-T细胞培养方法在技术上是可行的
4. 在GMP大规模生产设施中,一种简化的CAR-T细胞培养方法在技术上是可行的
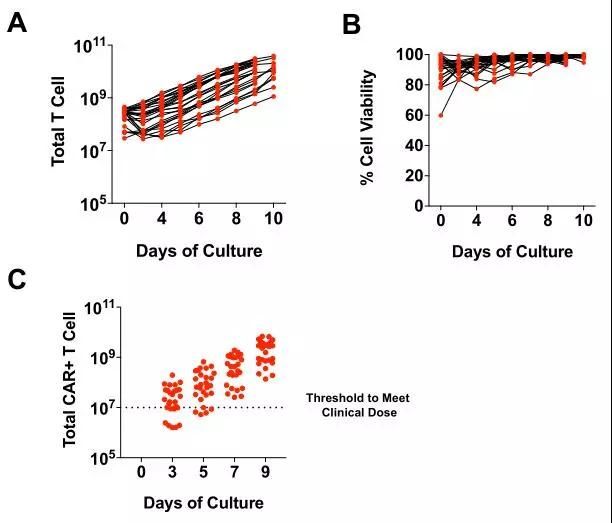 (A)CD19-BBζCAR转导活化的T细胞(T细胞来源于ALL患者)用anti-CD3 / CD28微珠刺激并使用大规模cGMP过程进行离体扩增,图表显示扩增期间的总T细胞数(n = 27个独立患者)。
(B) 对于A组患者,通过流式细胞术评估T细胞活性随时间的变化。
(C) 在扩增的第3、5、7和9天通过qPCR测量CD19-CAR丰度,用于临床应用的第9天收获的CAR+ T细胞的目标剂量由虚线表示。
研究结果及讨论
总而言之,离体培养期间发生的进行性分化与过继转移的T细胞的长期植入和总体有效率降低相关。先前已经报道了许多干预措施,以防止T细胞扩增期间发生的分化,例如阻断Fas-FasL相互作用、Akt抑制或Wnt信号的激活。
尽管这些方法能够阻碍细胞分化,但是与该研究团队所证明的相比,减少离体培养持续时间既简单又更具成本效益,这对于该技术的临床广泛应用是很重要的。
另外,研究过程中,该团队未观察到离体培养期间Tscm(记忆性干细胞样T细胞)的增加。而是在9天的培养期间维持数量,但频率降低了。结果显示:与第3天的产品相比,在第9天产品中过继转移的Tscm细胞的数量成比例地减少,这可能解释了更广泛培养的产品的长期植入和功效的降低(逆转录病毒载体)。
而将这种方法应用于慢病毒载体可以更深入地了解稳健和长期植入所需的T细胞亚群。研究人员提供证据表明,相对于第9天的CART19细胞,在第3天收获的CART19细胞在用其同源配体再刺激后具有增强的增殖能力。
虽然推测的第9天CAR T细胞可能表现出增殖能力减弱,是由于在培养过程中长时间暴露于激动性anti-CD3/CD28磁珠而导致T细胞耗尽的特征。但研究表明,通过缩短离体T细胞刺激的持续时间,T细胞具有增强的增殖和分泌效应细胞因子的能力,并且具有优异的抗肿瘤活性。而且,与临床观察结果一致,研究人员已经证明通过缩短制造过程产生的CAR T细胞含有更大比例的干细胞样T细胞。
另外,在较短时间内产生具有优异治疗潜力的细胞对CAR-T细胞制造也具有重要意义。毕竟延长的培养时间是昂贵的并且可能是多余的。除了减少劳动力之外,更有限的离体培养过程还能够节省稀缺的制造材料,例如人血清。尽管在无血清培养基中培养CAR-T细胞的方法正在开发中,但这些T细胞的有效性尚未确定。
目前的FDA指南还要求对转导后培养期大于96小时的进行复制能力的慢病毒/逆转录病毒检测。而采用短于5天的培养期将避免这种昂贵的测试。最后,更重要的是,缩短细胞提取和再输注T细胞产物之间的时间对于治疗患者尤其是快速进展性疾病的患者具有重要意义。
总之,该项最新的研究结果证明,缩短培养CAR-T细胞的持续时间,能够产生具有较少分化的T细胞产物,并显著增强其效应功能和增殖能力。进而导致体内抗白血病活性增强。在该研究团队的cGMP设施中制造的CAR T细胞的回顾性分析中,显示在第3天收获的细胞符合现有的第9天标准,能够满足70%的ALL患者的输注,进一步支持该个性化的可行性和直接转化潜力。
(A)CD19-BBζCAR转导活化的T细胞(T细胞来源于ALL患者)用anti-CD3 / CD28微珠刺激并使用大规模cGMP过程进行离体扩增,图表显示扩增期间的总T细胞数(n = 27个独立患者)。
(B) 对于A组患者,通过流式细胞术评估T细胞活性随时间的变化。
(C) 在扩增的第3、5、7和9天通过qPCR测量CD19-CAR丰度,用于临床应用的第9天收获的CAR+ T细胞的目标剂量由虚线表示。
研究结果及讨论
总而言之,离体培养期间发生的进行性分化与过继转移的T细胞的长期植入和总体有效率降低相关。先前已经报道了许多干预措施,以防止T细胞扩增期间发生的分化,例如阻断Fas-FasL相互作用、Akt抑制或Wnt信号的激活。
尽管这些方法能够阻碍细胞分化,但是与该研究团队所证明的相比,减少离体培养持续时间既简单又更具成本效益,这对于该技术的临床广泛应用是很重要的。
另外,研究过程中,该团队未观察到离体培养期间Tscm(记忆性干细胞样T细胞)的增加。而是在9天的培养期间维持数量,但频率降低了。结果显示:与第3天的产品相比,在第9天产品中过继转移的Tscm细胞的数量成比例地减少,这可能解释了更广泛培养的产品的长期植入和功效的降低(逆转录病毒载体)。
而将这种方法应用于慢病毒载体可以更深入地了解稳健和长期植入所需的T细胞亚群。研究人员提供证据表明,相对于第9天的CART19细胞,在第3天收获的CART19细胞在用其同源配体再刺激后具有增强的增殖能力。
虽然推测的第9天CAR T细胞可能表现出增殖能力减弱,是由于在培养过程中长时间暴露于激动性anti-CD3/CD28磁珠而导致T细胞耗尽的特征。但研究表明,通过缩短离体T细胞刺激的持续时间,T细胞具有增强的增殖和分泌效应细胞因子的能力,并且具有优异的抗肿瘤活性。而且,与临床观察结果一致,研究人员已经证明通过缩短制造过程产生的CAR T细胞含有更大比例的干细胞样T细胞。
另外,在较短时间内产生具有优异治疗潜力的细胞对CAR-T细胞制造也具有重要意义。毕竟延长的培养时间是昂贵的并且可能是多余的。除了减少劳动力之外,更有限的离体培养过程还能够节省稀缺的制造材料,例如人血清。尽管在无血清培养基中培养CAR-T细胞的方法正在开发中,但这些T细胞的有效性尚未确定。
目前的FDA指南还要求对转导后培养期大于96小时的进行复制能力的慢病毒/逆转录病毒检测。而采用短于5天的培养期将避免这种昂贵的测试。最后,更重要的是,缩短细胞提取和再输注T细胞产物之间的时间对于治疗患者尤其是快速进展性疾病的患者具有重要意义。
总之,该项最新的研究结果证明,缩短培养CAR-T细胞的持续时间,能够产生具有较少分化的T细胞产物,并显著增强其效应功能和增殖能力。进而导致体内抗白血病活性增强。在该研究团队的cGMP设施中制造的CAR T细胞的回顾性分析中,显示在第3天收获的细胞符合现有的第9天标准,能够满足70%的ALL患者的输注,进一步支持该个性化的可行性和直接转化潜力。
(本文来源生物谷)
想要了解更多请关注“中洪博元医学实验帮
参考出处:
http://cancerimmunolres.aacrjournals.org/content/early/2018/07/20/2326-6066.CIR-17-0405
DOI: 10.1158/2326-6066.CIR-17-0405




